
药物毒理学的创新:质谱成像技术的应用
药物毒理学的创新:质谱成像技术的应用
2021年12月,北京协和医学院药物研究所贺玖明、靳洪涛团队在Toxicology(《毒理学》)杂志发表了题为“Innovation in drug toxicology: Application of mass spectrometry imaging technology”的综述文章,系统的介绍该技术在药物及代谢产物的组织分布研究、药物器官(肝、肾、肺和中枢神经系统等重要器官)毒性研究、结合组学技术前沿方法发现毒性生物标志物和阐释药物毒性作用机制,展示了该技术在药物毒理学研究领域中的独特优势和广阔前景。
1.引言
安全性和有效性是药物属性的两个方面,在新药开发的整个过程中进行药物毒性筛选,可以显著降低毒副作用,减少研发投入,缩短开发周期,提高上市成功率。同时,药物毒性研究可以为指导临床合理用药,减少患者给药后的毒副作用提供相关数据和依据。药物毒理学中研究药物及其代谢产物在组织内的特异性分布和定量检测有助于寻找药代动力学规律,定位药物和代谢产物的分布蓄积以及探究药物对机体的作用以及潜在的毒性机制。
目前定性定量检测药物分布的方法主要是定量全身放射自显影技术(QWBA)、组织匀浆液质(LC/MS)分析,荧光标记以及免疫组化等方法。然而,QWBA和荧光标记无法区分药物和代谢物,LC/MS灵敏度较高但无法保留原位信息,而免疫组织化学具有高度特异性但仅限于可获得抗体的分子且只能测量单个靶标的生物分布,新兴的质谱成像技术可同时克服上述局限,在保证原位空间信息的基础上提供化合物的相对丰度信息,同时发挥定性、定量和定位功能,无需放射性核素或荧光标记,可以对已知未知分子同时进行高通量检测成像,具有高分辨率,高灵敏度,高特异性,质量范围宽,实验周期短等特点。本文总结了近年来质谱成像技术在药物毒理学领域的多种应用,展现了该技术应用于器官毒性研究中定性定量检测药物及代谢产物的特征性分布,肯定了质谱成像技术应用在组学领域推动毒性生物标志物的发现以及毒性机制见解方面的新兴作用。

2.质谱成像简介
质谱成像技术集成质谱分析与图像处理功能,其基本原理是将待测样品表面的多种分子按空间位置通过质谱仪进行离子化并检测,获取的多维数据利用图像软件可视化处理后得成像结果。
以肾脏组织作为样品分析对象简述质谱成像技术的流程(见下图):首先制作冷冻组织切片(一般15-20μm),依据研究目标分子的类型选择适合的成像探针、质谱分析器和扫描方式并对实验参数进行优化,质谱仪按照预先设定的程序利用激光或高能粒子束轰击样本使样品表面分子或离子解析离子化,气态离子经过质量分析器后采集到各像素点离子的原始质谱数据,最后借助图像处理软件将质谱峰的质荷比、离子强度和空间位置综合成像获得分布图。

图1. 质谱成像技术流程图
3.质谱成像在药物毒理学中的应用
3.1器官毒性:毒性药物代谢分布
3.1.1肾脏毒性
肾脏是药物排泄的首要器官,药物引起的肾毒性常见于所有患者的临床用药中,药物及代谢产物或因其引起的生理扰动(例如pH变化)导致内源性成分在肾脏中结晶形成沉积物是引起肾毒性的常见原因之一,通过组织病理初步检查后可用质谱成像方法检测结晶物质的分布以及确定结晶化合物的组成。

图2. 质谱成像可视化兔肾脏组织中药物化合物(m/z 378)及代谢物空间分布
3.1.2肝脏毒性
肝脏是机体主要的代谢器官也是人体的解毒工厂,药物引起的肝毒性是临床用药最常见的副作用之一,对乙酰氨基酚(APAP)被报道在肝小叶的中央周围区域会引起肝毒性,MALDI-MSI可视化APAP及其代谢物存在于特定的小叶区域,APAP–GSH加合物和GSH消耗主要发生在肝脏的CYP2E1阳性区域,APAP、APAP-硫酸盐(SUL)、APAP-葡萄糖醛酸(GLC)和APAP-GSH加合物呈剂量依赖性增加而GSH呈剂量依赖性消耗。
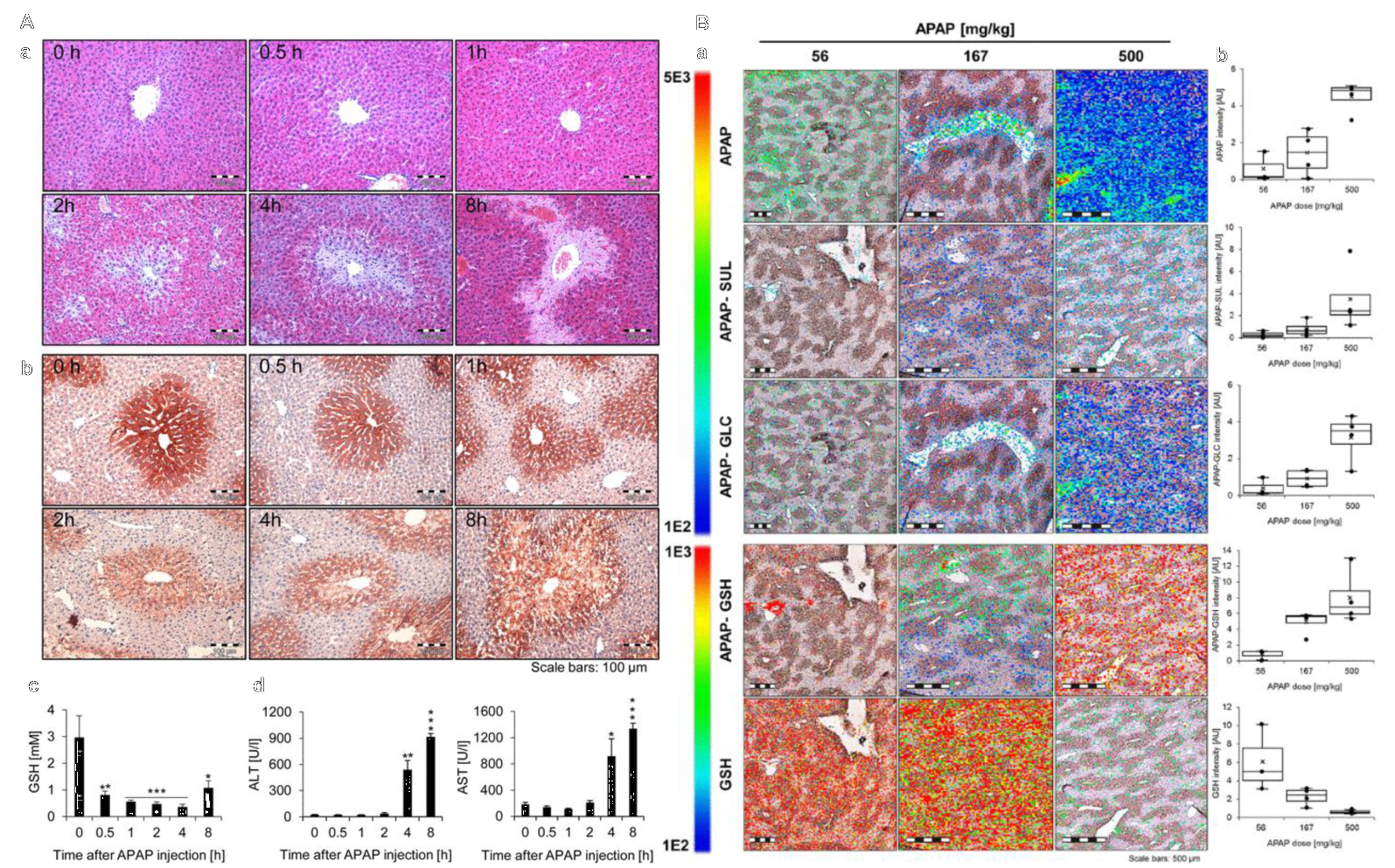
图3. MALDI-MSI可视化APAP及其代谢物存在于特定的小叶区域分布
3.1.3 肺脏毒性
药物对呼吸系统的毒性作用可能引起急性化学性肺炎和慢性肺纤维化,甚至出现呼吸衰竭危及生命,对药物肺毒性的研究值得关注。质谱成像可对药物精确量化以跟踪其在特定器官和组织隔间内的运输状态。研究发现在给药后15分钟内,噻托溴铵母离子和碎片子离子以80fmol-5pmol浓度梯度从中央气道分散到肺实质还有胸膜,质谱成像定量和定性地测定靶向组织的体内药物吸收,为药物存在部位发生的动态生物过程提供了支持。
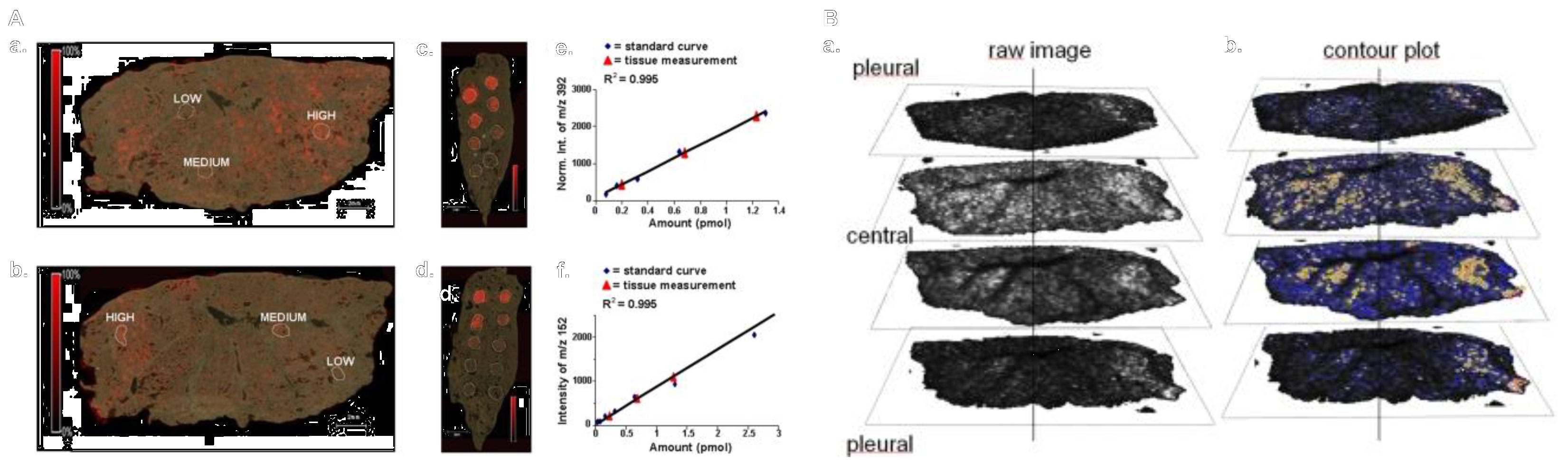
图4. 吸入噻托溴铵在连续切片大鼠肺组织中的空间分布
3.1.4 神经毒性
大脑是人体最为复杂的器官,药物可通过血脑屏障进入大脑产生神经毒性,质谱成像尤其适用于反映药物在大脑分区中的分布,质谱成像和LC-MS创造性应用于比较药物通过血脑屏障的渗透能力以及确定其在脑中动力学参数的和空间特异性分布。研究报道三种一线抗逆转录病毒药物(依非韦伦,替诺福韦和恩曲他滨)在脑中的区域性分布以指导临床联合用药。
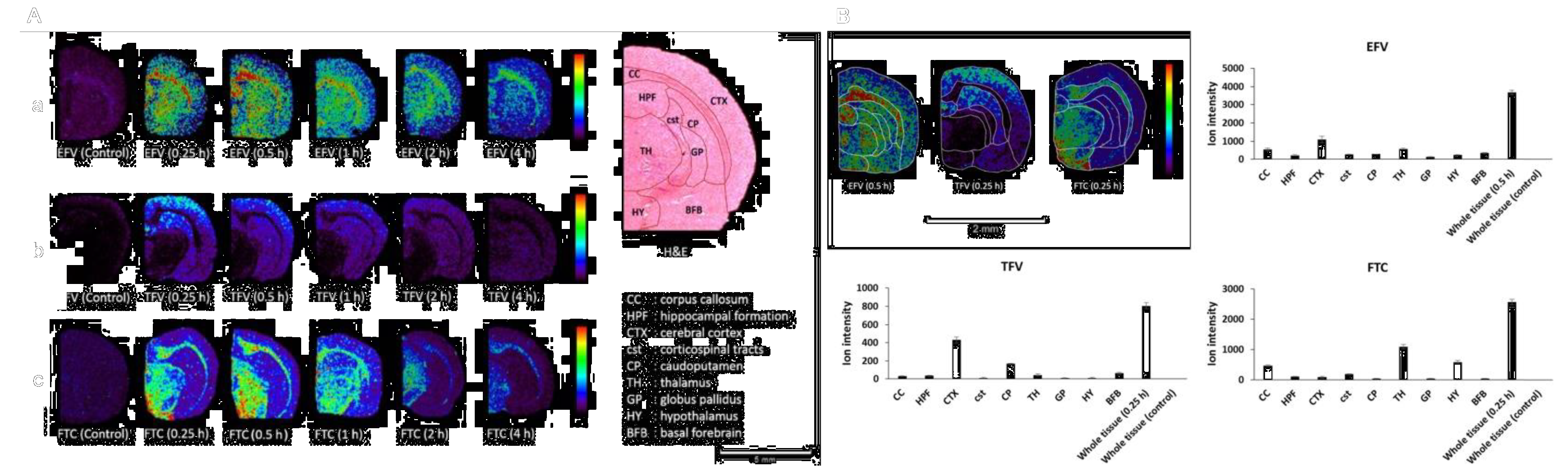
图5.质谱成像描绘三种一线抗逆转录病毒药物在脑区域分布模式
3.2 生物标记物及毒理学机制
质谱成像无需分离纯化便可以对已知和未知的分子同时成像分析提供空间分布和相对含量信息,其分子识别能力和无标记生物分子成像的特点为生物标记物发现提供了新策略,广泛应用在蛋白质组学,代谢组学和脂质组学等领域。药物的毒性机制涉及药物的作用通路与相关的靶点,通过对比给药前后体内的代谢产物、脂质、蛋白质的差异变化,从而寻找药物毒性相关的生物标志物,预测和评估药物毒性。
3.2.1 蛋白质组学
蛋白质是人体生理功能的执行者,反映了生物体正在发生的事件,是基因最终真实表达形式,研究整套的蛋白质组学可直接阐明机体在生理或病理条件下的变化机制,是寻找生物标志物和药物靶标最有效的方法之一。MALDI质谱成像发现给药后的大鼠中肾脏皮质,髓质和乳头中的蛋白质表达有明显差异,例如甲状腺素运载蛋白( m/z 12,959 )水平在皮质中明显升高,结合蛋白质印迹分析和免疫组织化学方法确证甲状腺素运载蛋白为庆大霉素诱导的大鼠肾毒性的生物标志物。
3.2.2代谢组学
相较于蛋白质组学,代谢组学侧重的是机体已经发生的事情,通过检测小分子代谢物的变化寻找内源性代谢物与生理病理变化的相对关系,从而加深我们对疾病机理的了解,加快发现生物标志物以及阐明药理毒理作用机理。马兜铃酸被报道就有肾毒性。质谱成像发现马兜临酸的的肾毒性与精氨酸-肌酸代谢,胆碱代谢紊乱,以及脂质代谢有关。

图6. 质谱成像揭示马兜铃酸诱导的肾毒性代谢标志物和通路变化
4.展望
质谱成像技术可以准确地检测组织中无标记的内源性或外源性分子,不仅用于药物及代谢产物的同时分布定量研究,还可用于组学技术研究发现毒性生物标志物,确定药物的代谢通路和潜在毒性机制。随着质谱成像技术的进一步发展将赋予其在药物毒理学领域更为广阔的发展前景,并将有力地推动药物毒理学领域的新发现。
中国医学科学院药物研究所博士生江海燕为本文第一作者,高杉杉,胡广为本文共同作者,贺玖明研究员和靳洪涛研究员为本文通讯作者。本工作得到国家自然科学基金(81773996, 81773678, 81973476),国家重大科技专项“重大新药开发”项目(2018ZX09735006, 2018ZX09711001002-001, 2018ZX09201017-005)和中国毒理学学会临床毒理学转化研究项目(CST2019CT105)的资助。
全文链接:Innovation in drug toxicology: Application of mass spectrometry imaging technology - ScienceDirect


